Нікелю сульфат. Хімічне нікелювання.

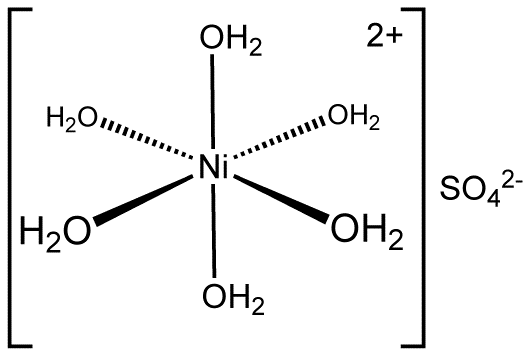
Нікель сірчанокислий (гексагідрат сульфату нікелю) - добре розчинна у воді сіль синьо-зеленого кольору. Кристалогідрат тетрагональної будови, у водних розчинах існує у виглядів іонів [Ni(H2O)6]2+, pKa - 4,5. Трапляється у природі у вигляді мінералу ретгерциту. Найбільше використовується для нікелювання металів та сплавів. Також для виготовлення акумуляторів, каталізаторів,тощо в електронній та електротехнічній галузях.
Хімічне нікелювання
Нікелеві покриття підвищують стійкість виробів проти зношування, захищають їх від корозії як в атмосферних умовах, так і в агресивних хімічних середовищах, надають їм декоративного вигляду. Нікелювання застосовують у виробництві хімічної апаратури, медичних інструментів, автомобілів і велосипедів, побутових виробів тощо.
Нікель наносять найчастіше електролітичним способом, рідше – хімічним. Недоліками електролітичного нікелювання є нерівномірність осадження нікелю на рельєфній поверхні та неможливість покриття вузьких і глибоких отворів, порожнин тощо. Хімічне нікелювання є дещо дорожчим за електролітичне, проте забезпечує можливість нанесення рівномірніщого за товщиною і якістю покриття на будь-які ділянки рельєфної поверхні за умови доступу до них розчину.
Хімічним шляхом можна покривати нікелем більшість металів, крім свинцю, олова, кадмію та їх сплавів. В основі процесу хімічного нікелювання лежить реакція відновлення нікелю з водних розчинів його солей натрій гіпофосфітом в лужному або кислому середовищах. В результаті може утворитись блискуче або напівблискуче нікелеве покриття (сплав нікелю і фосфору з аморфною структурою).
Блискучі нікелеві покриття складаються з матового нікелевого покриття, над яким осаджують шар блискучого нікеля. Наявність двох роздільно осаджених шарів нікелю зменшує пористість покриттів. Блискуче нікелеве покриття є протектором і створює електрохімічний захист матового нікелевого покриття. Воно має більш негативний потенціал в порівнянні з матовим, і в гальванічному елементі, що утворюється в корозійному середовищі, відіграє роль анода. Щоб зменшити пористість покриттів і тим самим поліпшити їх захисну здатність, застосовують попереднє латунування, міднення або наносять багатошарові покриття (наприклад: мідь-нікель-хром).
Плівка нікелю без додаткової термообробки слабко тримається на поверхні основного металу, хоча її твердість близька до твердості хромового покриття. Це обумовлено наявністю фосфору. Вміст фосфору в покритті залежить від складу розчину нікелювання і змінюється в межах від 4-6% для лужних розчинів до 8-10% для кислих розчинів. Термічна обробка деталі з нікелевим покриттям (нагрівання до температури 350-500 °С понад 1 год.) значно збільшує зчеплення плівки нікелю з основним металом, одночасно з цим зростає і твердість нікелю.

Для проведення хімічного нікелювання застосовують кислотні та лужні розчини. Лужні розчини характеризуються стійкістю в роботі, легкістю коректування складу, можливістю тривалого використання без заміни, майже повною відсутністю явища саморозряду, яке є типовим для кислотних розчинів. Саморозряд полягає в миттєвому осіданні губчастої маси нікелю, яке відбувається при перегріванні розчину і супроводжується викидом киплячої суміші з ванни. Проте твердість покриття виробів з лужних розчинів приблизно на 15% нижче, ніж з кислотних. Нижчою є і корозійна стійкість таких покриттів. Тому частіше застосовують нікелювання з кислих розчинів.
Підготовка поверхні перед хімічним нікелюванням полягає в її травленні в суміші кислот. Нікелювання алюмінію і його сплавів здійснюють після цинкатної обробки, яку повторюють двічі, в лужному середовищі у присутності сполук цинку (температура розчину – 20 °C, час обробки – 3-5 с). Хімічне нікелювання проводять при температурі 85-95°С у водних розчинах, що містять гіпофосфіт натрію (калію), нікелеві солі та інші речовини. Швидкість осадження нікелю становить 10-20 мкм/год. Виділяється щільний блискучий осад, який складається з твердого розчину нікелю та містить 5-13% фосфору і має твердість 300-350 HV. Подальший відпал при 400 °С підвищує твердість покриття до 600-800 HV і покращує його зчеплення з основним металом.
Кислотний розчин для хімічного нікелювання металів та їх сплавів
Вміст складових у розчині
-
Нікель сульфат 20-40 г/л
-
Натрій сульфат 10-20 г/л
-
Натрій гіпофосфіт 10-20 г/л
-
Оцтова кислота 1-3 мл/л
Особливості нікелювання
- Швидкість покриття 10 мкм/год
- Температура 87-92 °С
Розчин для нікелювання готується наступним чином:
Нагріваємо воду до температури 70 °С і розчиняємо нікель сульфат, оцтову кислоту (ρ = 1,05 г/л), додаємо воду до 1 л. Нагріваємо отриманий розчин до робочої температури 89 ± 2°С і вводимо натрій сульфат. Розчин має рН = 4,1-4,3. Потім опускаємо попередньо підготовлену пластинку з алюмінію, його сплаву, міді, її сплаву або сталі. Про початок реакції свідчить виділення бульбашок водню на поверхні металу.
Коригування розчину здійснюють за значенням рН і за вмістом гіпофосфіту натрію, тому що зміна концентрації солі нікелю незначно впливає на швидкість процесу.
Перевірка міцності зчеплення покриття з основним металом проводиться методом зміни температур (термоудару) в електропечі при температурі 200 °С протягом 30 хвилин і зануренням в воду з температурою 15-25 °С. Зчеплення покриття з металом вважається хорошим, якщо не відбувається відшаровування або здуття покриття.
Процес нікелювання йде стабільно і з великим приростом товщини покриття до 4 годин і далі потрібне коригування розчину, після якого процес стабільний протягом 2 годин, тобто загальний час ефективної роботи розчину становить 6 годин. Коригування розчину проводиться кожні 30 хвилин додаванням 4 мл/л 10%-го розчину натрій гідроксиду, уникаючи попадання лугу на деталі і розрахункової кількості гіпофосфіту натрію.

Нікелювання у псевдорозрідженому шарі інертних частинок
Одним з найбільш ефективних та перспективних методів інтенсифікації електрохімічних процесів є електроліз у псевдозрідженому шарі інертних часток (ПЗШ ІЧ), який дозволяє отримувати компактні осади металів з кращими властивостями та з підвищеною продуктивністю. Однак широке застосування методу гальмується деякою складністю та обмеженістю використання, відсутністю систематизованих даних про вплив ПЗШ ІЧ на окремі електрохімічні процеси, в тому числі нікелювання.
Для осадження нікелевого покриття використовується електроліт такого складу (г/дм3): нікелю сульфат – 200; кислота борна – 25; натрію хлорид – 25. Режим електролізу: pH – 5–5,5, температура 50 °С. У звичайному режимі електролізу здійснюється перемішування електроліту стислим повітрям, густина струму складала 2 А/дм2. Режим псевдозрідження створюється за допомогою насосу, як інертні частки використовуються поліровані скляні кульки діаметром 1–1,3 мм, якими на дві третини об’єму заповнюється гальванічна ванна. Швидкість потоку забезпечує оптимальну відносну ступінь розширення щільного шару інертних часток близько 1,5. Турбулентний режим перемішування забезпечуває співударяння твердих часток з поверхнею катоду, що сприяє утворенню центрів кристалізації (дрібнокристалічності осадів) і дозволяє підвищити робочу густину струму (відповідно, і продуктивність процесу).
Покриття, які були отримані у ПЗШ ІЧ, у порівнянні з покриттями, одержаними у звичайному режимі, відрізняються кращим зовнішнім виглядом (блиском) та кращою дрібнокристалічністю, що пояснюється механічним впливом інертних часток, а також збільшенням кількості центрів кристалізації. При використанні ПЗШ ІЧ може бути суттєво збільшена робоча густина струму без погіршення властивостей нікелевого осаду. Збільшення продуктивності пояснюється тим, що при електролізі у ПЗШ ІЧ збільшується значення граничного дифузійного струму. Також покращується розсіювальна здатність при використання ПЗШ ІЧ, що пояснюється збільшенням перенапруги виділення нікелю.
- Хімія для роботи з чорними та кольоровими металамиРекомендації щодо проведення хімічної підготовки металів для подальшої роботи з нимиХімія для роботи з чорними та кольоровими металами
- Лимонна кислота: застосування у харчовій промисловості, побуті та інших сферахЛимонна кислота – універсальний інгредієнт, який широко використовується в харчовій промисловості, косметології, медицині та побуті. Дізнайтеся, як вона допомагає зберігати продукти, очищати поверхні та покращувати якість випічки. У цій статті ми розглянемо її основні властивості та ефективне застосування.Лимонна кислота: застосування у харчовій промисловості, побуті та інших сферах






